La mycoplasmose bovine aujourd'hui et demain
L’édition du Sillon Belge du 20 juin 2024 vous présentait un dossier consacré à la mycoplasmose bovine, depuis sa description jusqu’aux solutions existantes, en passant par la détection et la prévention au sein de nos troupeaux d’animaux. Dès lors, à présent, quoi de neuf en termes de prévalence, de diagnostic et de contrôle de cette maladie ?

Une étude rétrospective de l’Arsia, menée en 2016 par son département épidémiologie et encadrement sanitaire, a confirmé la présence de Mycoplasma bovis (M.bovis) dans au moins un tiers des troupeaux viandeux et mixtes wallons selon des fluctuations annuelles importantes, et l’augmentation de sa circulation entre 2012 et 2016. Le germe était présent également dans les troupeaux laitiers, à raison d’un élevage sur quatre.
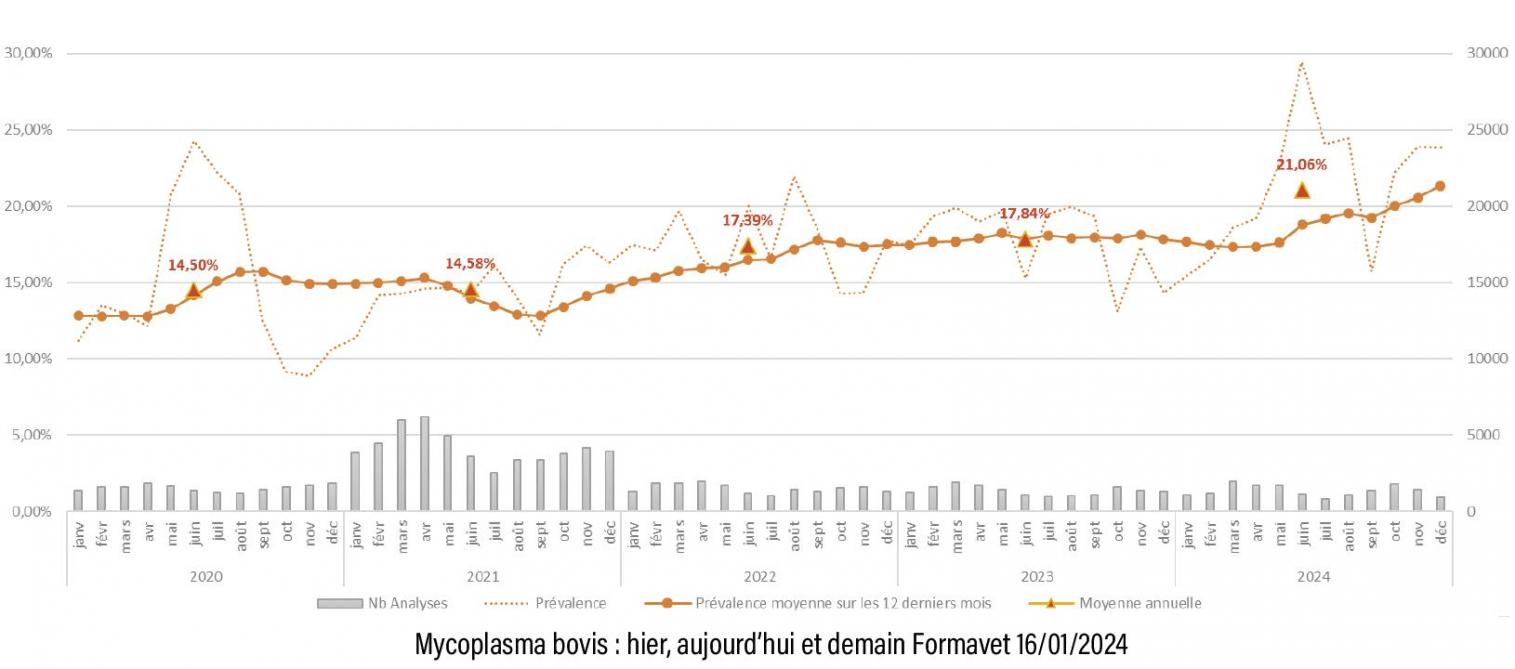
Deux autres indicateurs édifiants sont les « kit achat » et « kit respiratoire », proposés et réalisés par l’Arsia et son laboratoire. Les résultats du premier révèlent la présence croissante d'anticorps contre M. bovis chez les animaux testés dans le cadre du protocole d'achat, entre 2020 et 2024. Pour le second, près de 25 % des échantillons sont testés positifs chaque année (et environ 30 % à l’échelle du troupeau).
La mycoplasmose est donc endémique en Belgique qui n’est pas la seule concernée, loin de là. Pour en venir à bout, de nombreux pays européens travaillent sur des plans de contrôle ou de lutte. Le défi est de taille, mais il est n’est pas insurmontable... Des pistes existent comme en atteste dans cet article une nouvelle approche reposant sur l’imagerie médicale, développée à l’Université de Gand.
Une bactérie particulière
M. bovis se décline selon plus de 100 espèces pathogènes. On la retrouve chez l’homme, les animaux et les plantes. De petite taille et dépourvue de paroi, elle n’en donne pas moins du fil à retordre aux vétérinaires et aux éleveurs. D’une part, de par ses caractéristiques, elle est insensible à 50 % des antibiotiques disponibles et développe toujours plus de résistances envers ceux qui peuvent être utilisés pour la combattre.
D’autre part, elle sévit fréquemment en association avec des agents infectieux secondaires.
Le diagnostic : qTUS, un outil au chevet des veaux
Docteur en sciences vétérinaires et spécialiste du Collège européen de gestion de la santé bovine, Bart Pardon est professeur en médecine interne des ruminants de l'Université de Gand (UGent).
Par ailleurs, son équipe propose des outils aux agriculteurs et aux vétérinaires, en se concentrant sur la santé des veaux en général, la santé respiratoire et la septicémie en particulier, dans le but de rationaliser l'utilisation des antimicrobiens. Leurs projets actuels comprennent le développement d'outils de diagnostic rapide, de soutien à la décision thérapeutique, d’applications de médecine de précision et l'évaluation d'interventions telles que la thérapie antimicrobienne et la vaccination contre les maladies respiratoires bovines. Une partie importante des travaux passés et présents de Bart Pardon traitent de Mycoplasma bovis , un intérêt né au cours de son doctorat dans l'industrie du veau.
En 2023, il a cofondé qTUS (quick Thoracic UltraSonography), une spin-off liée à l'UGent, travaillant avec l’échographie pulmonaire. Cette méthodologie est désormais enseignée aux étudiants et aux praticiens vétérinaires et largement utilisée dans les élevages flamands.
Quels en sont les tenants et aboutissants ?
Les élevages de veaux de boucherie présentent jusqu’à … 100 % de positivité à M. bovis . En effet, toute exploitation qui achète régulièrement des animaux est clairement et pleinement exposée au risque d’être infectée. D’où l’utilisation abondante des antibiotiques dans ces fermes, problème critique… et critiquable, dans le contexte de la lutte contre l’antibiorésistance.
Face à la mycoplasmose dans de tels élevages, le vétérinaire peut s’appuyer sur deux outils : l’imagerie médicale et le diagnostic par lavage broncho-alvéolaire ou écouvillonnage nasal profond. C’est ce qu’a développé l’UGent, via la spin-off qTUS, qui propose une approche diagnostique selon une séquence bien définie. Un animal tousse ? Ce seul signe suffit pour décider d’une échographie de ses poumons. En 2 à 3 minutes, sans rasage préalable nécessaire, un résultat rapide est obtenu, avec une sensibilité de 85 % et une spécificité de 95 %. Sachant que la sensibilité d’un test est sa capacité à détecter tous les malades, et donc d’avoir le moins de faux négatifs. La spécificité est, quant à elle, la capacité à ne détecter que les malades, et d’avoir le moins de faux positifs.
Le recours à l’échographie
Pourquoi recourir à un examen échographique au chevet des veaux en ferme ? Au terme d’études menées pendant plusieurs années par Bart Pardon, le constat est le suivant : dans un élevage ou sévit la mycoplasmose, sur base des seuls signes cliniques, détectés à un moment donné, il est impossible d'identifier de manière fiable les veaux réellement atteints de pneumonie.
Certains d’entre eux peuvent apparaître « normaux », alors qu’en réalité, à l’échographie, ils présentent une pneumonie. C’est la pneumonie « subclinique ». Selon l’estimation par le vétérinaire de son degré de sévérité, ce sont en réalité ces veaux qui ont besoin d’antibiotiques. D’autres jeunes présenteront de la fièvre… mais aucune lésion pulmonaire. Ils ne sont pas candidats à l’antibiothérapie ; on ne va pas traiter tous les animaux présentant des signes cliniques, lorsque ceux-ci sont en fait liés à l’inflammation des voies respiratoires supérieures et non des poumons. Cela correspond pleinement à une démarche responsable d’utilisation des antibiotiques.
En Flandre, selon une étude menée par Bart Pardon, près de 40 % des veaux sont classés « subcliniques ». 75 % d’entre eux présentent au moins un signe d’alerte… et donc 25 % aucun signe. D’où le grand intérêt de l’échographie qui permettra de les repérer et les traiter à temps et à heure.
Si dans les très grandes exploitations, il n’est évidemment pas possible de passer les jeunes bovins chaque jour à l’échographe, des systèmes d’alerte sanitaire existants, ou en voie de développement, peuvent indiquer les candidats à l’échographie.
Un autre apport précieux de cet examen en ferme est de pouvoir, sur base des images pulmonaires, confirmer la guérison effective de l’animal et arrêter l’antibiothérapie en connaissance de cause. L’échographie pulmonaire est une option réalisable pour chaque vétérinaire, sur base d’un apprentissage. La spin-off qTUS propose cette formation aux vétérinaires, combinant des cours en ligne et des sessions pratiques. La certification des compétences en échographie pulmonaire est, en effet, essentielle pour une utilisation responsable des antibiotiques et garantir la validité des labels de durabilité et de bien-être animal.
Lors de la première visite dans un élevage à problème, le diagnostic de laboratoire fait partie du protocole qTUS. Des lavages broncho-alvéolaires, réalisés sur cinq veaux dont les prélèvements sont analysés en pools, permettront une détection indirecte (sérologique) ou directe du ou des germes en présence (culture, PCR, technologie Maldi Tof pour permettre l’identification de très nombreuses bactéries en un délai très court, séquençages… ).
Ultérieurement, en cas de nouveaux cas dans l’exploitation ou d’une seconde flambée de pathologies respiratoires, des prélèvements pour le laboratoire seront d’emblée renouvelés. Ce ne sont ainsi pas forcément les mêmes germes qu’identifiés précédemment, lors d’une épidémie antérieure. Refaire un diagnostic au laboratoire est important !
La prévention repose sur la biosécurité externe
La biosécurité externe, c’est LE facteur clé : il s’agit de ne pas acheter une maladie ! Outre l’indispensable mise en quarantaine à l’achat de tout bovin, un test de détection des maladies potentielles (dont la mycoplasmose) est vivement recommandé. Selon le résultat, il s’agit ensuite pour l’éleveur de conclure ou non l’achat. Ce n’est pas tout blanc ou noir, comme on pourrait s’y attendre. Se pose la question de la valeur du résultat... Test positif… quelle est la probabilité qu’il soit vraiment positif ? Test négatif… quelle est la probabilité qu’il soit vraiment négatif ? Négatives ou positives, ces valeurs prédictives sont, en réalité, influencées par la prévalence (ou circulation) de la maladie. Le résultat « positif » ou « négatif » ne suffit pas en lui seul. Ainsi, chaque test (Elisa ou PCR) est caractérisé par un pourcentage de sensibilité et de spécificité. Il y a donc lieu de se reposer sur une interprétation du résultat, pondérée par ce pourcentage et la circulation réelle du germe (pour M. bovis , 30 % en Belgique) et menée avec le vétérinaire et/ou le laboratoire, pour décider de garder ou non le bovin.
Contrôler la maladie : traitement, biosécurité interne, réforme
Comment et pourquoi traiter ? M. bovis est le pathogène le plus présent dans les veaux de boucherie. Pour chaque veau clinique, il y a trois bêtes subcliniques, à l’image d’un iceberg. Et l’impact économique est important (retard de croissance, mortalités…). Constat toutefois encourageant pour le vétérinaire et son éleveur : un jeune soigné et guéri peut récupérer entièrement, sans perte de poids, alors qu’une pneumonie chronique entraîne une perte moyenne de 10,3 kg de poids de carcasse. Plus tôt on intervient, plus grandes sont les chances de récupération. En cas de pneumonie sévère, le traitement contre la mycoplasmose est long et lourd pour l’animal qui doit recevoir une injection par jour… et coûteux. Il s’agit là d’une décision à prendre en concertation vétérinaire ou/et l’éleveur.
Le passage à l’échographie permet une détection précoce, soutient la décision thérapeutique et raccourcit la durée du traitement.
Le spécialiste le reconnaît : pour casser une explosion de cette maladie dans un élevage, la métaphylaxie reste souvent nécessaire. Elle consiste à traiter les animaux cliniquement malades mais aussi ceux encore cliniquement sains d'un même groupe, sur base de la forte probabilité qu’ils soient infectés à cause du contact étroit avec les bêtes malades. Toutefois, à ce jour, la tendance générale est de limiter autant que possible cette approche thérapeutique, dans le cadre de la lutte contre l’antibiorésistance.
La biosécurité interne
Dès la naissance, le box de parturition est le lieu de tous les dangers lorsqu’il est partagé pour tous les vêlages. Une mère contaminée peut contaminer un autre veau que le sien en le léchant, par le jetage nasal.
Jusqu’à présent, le logement individuel des veaux était prôné, de façon assez évidente : diminuer le risque de contamination entre animaux malades et sains. Ce principe va toutefois devoir s’adapter aux nouvelles normes européennes liées au bien-être animal. L’avis scientifique de l’Efsa recommande les conditions d’élevage suivantes : entre autres, le logement minimum par deux, le veau doit rester avec sa mère 24 heures pour téter, groupes stables avec un maximum de 10 animaux ou encore transport autorisé à partir de 14 jours jusqu’à 28 jours.
Quant à l’alimentation, on ne distribue pas le lait d’une mère positive, ni le lait écarté, sources de contamination relativement importante. Une mère excrétrice qui contamine un lait de mélange peut infecter l’ensemble des veaux nourris.
Réforme ? Comme il est souvent conseillé, « un animal malade doit partir ». Il n’en reste pas moins que l’éleveur perd son bovin. Il faut être sûr de la décision de réformer. D’autant plus qu’à ce jour, souligne Bart Pardon, on ne dispose pas encore de la preuve d’un retour plus rapide à un statut négatif du troupeau, grâce aux réformes. En phase aiguë, un animal peut guérir, une élimination naturelle du mycoplasme est toujours possible le premier mois. On décrit également des auto-guérissons pendant le tarissement (86,7% des animaux positifs guérissent sans antibiotiques !).
Après le début d’une épidémie dans un élevage, le spécialiste conseille dans tous les cas d’attendre 2 mois minimum avant d’initier une stratégie de tests appropriés et de réforme. Chez le veau, l’estimation de la gravité de la pneumonie pourra également être évaluée par échographie.
Sont toutefois voués à la réforme : les veaux avec pneumonie réfractaire (à confirmer par échographie), les vaches avec mammites cliniques et mammites subcliniques chroniques à M. bovis , et les vaches avec pneumonie chronique ou arthrite.
Et la vaccination ? Un premier vaccin vivant dirigé contre M. bovis destiné aux bovins à partir d’une semaine d’âge est maintenant disponible. Il va probablement modifier les paramètres en termes d’immunisation, de contrôle et de suivi des troupeaux. Pour les situations où ce vaccin vivant ne pourra pas être utilisé, il existera toujours la possibilité de recourir aux autovaccins, outil intéressant et efficace dans le contrôle de la mycoplasmose bovine.





